Закон радиоактивного распада
Содержание:
- Примеры значений и уравнений
- Токсичность
- Как действовать?
- Источники полония
- Временной интервал в радиоактивности
- Получение
- Примечания
- Бизнес и финансы
- Примеры характеристик распада
- Примеры
- Определение и основные соотношения
- Виды частиц, испускаемых при радиоактивном распаде
- Виды радиоактивного распада: α-распад, β-распад. Характеристики радиоактивных излучений.
Примеры значений и уравнений
| Характерная черта | Описание | Условное обозначение | Ед. изм | Формула | Рабочий пример значения |
|---|---|---|---|---|---|
| Доза | Количество введенного препарата. | D{\ displaystyle D} | мол{\ Displaystyle \ mathrm {mol}} | Расчетный параметр | 500 ммоль |
| Интервал дозирования | Время между введениями дозы препарата. | τ{\ Displaystyle \ тау} | s{\ Displaystyle \ mathrm {s}} | Расчетный параметр | 24 ч |
| C макс | Пиковая концентрация препарата в плазме крови после приема. | CМаксимум{\ displaystyle C _ {\ text {max}}} | M{\ Displaystyle \ mathrm {M}} | Прямое измерение | 60,9 ммоль / л |
| t макс | Время достижения C макс . | тМаксимум{\ Displaystyle т _ {\ текст {макс}}} | s{\ Displaystyle \ mathrm {s}} | Прямое измерение | 3.9 ч |
| C мин | Низкая ( корыта ) концентрация , что лекарственное средство достигает до следующей дозы вводят. | Cмин,сс{\ displaystyle C _ {{\ text {min}}, {\ text {ss}}}} | M{\ Displaystyle \ mathrm {M}} | Прямое измерение | 27,7 ммоль / л |
| Объем распространения | Кажущийся объем, в котором распределено лекарство (т.е. параметр, связывающий концентрацию лекарственного средства в плазме с количеством лекарственного средства в организме). | Vd{\ displaystyle V _ {\ text {d}}} | м3{\ Displaystyle \ mathrm {м} ^ {3}} | DC{\ displaystyle {\ frac {D} {C_ {0}}}} | 6.0 л |
| Концентрация | Количество препарата в заданном объеме плазмы . | C,Cсс{\ displaystyle C_ {0}, C _ {\ text {ss}}} | M{\ Displaystyle \ mathrm {M}} | DVd{\ displaystyle {\ frac {D} {V _ {\ text {d}}}}} | 83,3 ммоль / л |
| Период полураспада | Время, необходимое для того, чтобы концентрация препарата удвоилась по сравнению с исходным значением для перорального и других внесосудистых путей введения. | т12а{\ displaystyle t _ {{\ frac {1} {2}} а}} | s{\ Displaystyle \ mathrm {s}} | пер(2)kа{\ Displaystyle {\ гидроразрыва {\ ln (2)} {к _ {\ текст {а}}}}} | 1.0 ч |
| Константа скорости абсорбции | Скорость, с которой лекарство попадает в организм при пероральном и других внесосудистых путях. | kа{\ Displaystyle к _ {\ текст {а}}} | s-1{\ Displaystyle \ mathrm {s} ^ {- 1}} | пер(2)т12а{\ displaystyle {\ frac {\ ln (2)} {т _ {{\ frac {1} {2}} а}}}} | 0,693 -1 |
| Период полувыведения | Время, необходимое для того, чтобы концентрация препарата достигла половины исходного значения. | т12б{\ displaystyle t _ {{\ frac {1} {2}} b}} | s{\ Displaystyle \ mathrm {s}} | пер(2)kе{\ Displaystyle {\ гидроразрыва {\ ln (2)} {к _ {\ текст {е}}}}} | 12 часов |
| Константа скорости удаления | Скорость, с которой лекарство выводится из организма. | kе{\ displaystyle k _ {\ text {e}}} | s-1{\ Displaystyle \ mathrm {s} ^ {- 1}} | пер(2)т12бзнак равноCLVd{\ displaystyle {\ frac {\ ln (2)} {t _ {{\ frac {1} {2}} b}}} = {\ frac {CL} {V _ {\ text {d}}}}} | 0,0578 ч -1 |
| Скорость инфузии | Скорость инфузии, необходимая для баланса выведения. | kв{\ displaystyle k _ {\ text {in}}} | молs{\ Displaystyle \ mathrm {моль / с}} | Cсс⋅CL{\ displaystyle C _ {\ text {ss}} \ cdot CL} | 50 ммоль / ч |
| Площадь под кривой | Интеграл кривой концентрация-время (после однократной дозы или в стационарном состоянии). | АUC-∞{\ displaystyle AUC_ {0- \ infty}} | M⋅s{\ Displaystyle \ mathrm {M} \ cdot \ mathrm {s}} | ∫∞Cdт{\ displaystyle \ int _ {0} ^ {\ infty} C \, \ operatorname {d} t} | 1320 ммоль / л · ч |
| АUCτ,сс{\ displaystyle AUC _ {\ tau, {\ text {ss}}}} | M⋅s{\ Displaystyle \ mathrm {M} \ cdot \ mathrm {s}} | ∫тт+τCdт{\ displaystyle \ int _ {t} ^ {t + \ tau} C \, \ operatorname {d} t} | |||
| Оформление | Объем плазмы, очищенной от препарата за единицу времени. | CL{\ displaystyle CL} | м3s{\ Displaystyle \ mathrm {м} ^ {3} / \ mathrm {s}} | Vd⋅kезнак равноDАUC{\ displaystyle V _ {\ text {d}} \ cdot k _ {\ text {e}} = {\ frac {D} {AUC}}} | 0,38 л / ч |
| Биодоступность | Системно доступная фракция лекарственного средства. | ж{\ displaystyle f} | Безразмерный | АUCpo⋅DivАUCiv⋅Dpo{\ displaystyle {\ frac {AUC _ {\ text {po}} \ cdot D _ {\ text {iv}}} {AUC _ {\ text {iv}} \ cdot D _ {\ text {po}}}}} | 0,8 |
| Колебания | Пиковые колебания минимума в пределах одного интервала дозирования в установившемся режиме. | %пТF{\ displaystyle \% PTF} | %{\ displaystyle \%} |
CМаксимум,сс-Cмин,ссCсредний,сс⋅100%{\ displaystyle {\ frac {C _ {{\ text {max}}, {\ text {ss}}} — C _ {{\ text {min}}, {\ text {ss}}}} {C _ {{\ текст {av}}, {\ text {ss}}}}} \ cdot 100 \%}
|
41,8% |
Токсичность
У рассматриваемого элемента очень большая удельная активность – целых 166 ТБк/г. Под данным термином подразумевается количество осуществляемых в единицу времени радиоактивных распадов – спонтанного изменения состава или внутреннего строения атомных ядер.
Данное вещество излучает только альфа-частицы – положительно заряженные, образованные 2 протонами и 2 нейтронами. Но даже несмотря на это, его запрещено брать руками. Коснувшись этого мягкого серебристо-белого металла, человек гарантированно заработает лучевое поражение кожи как минимум. И высока вероятность того, что оно распространится по всему организму. Потому что изотоп легко проникает внутрь через кожные покровы.
Опасен он и на расстоянии, которое превышает длину преодоления альфа-частиц. Все потому, что они начинают самостоятельно нагреваться, вследствие чего переходят в аэрозольное состояние.
Это что касательно токсичности и распада полония-210. Но еще есть изотопы 208 и 209 – более долгоживущие. У 208-го период полураспада составляет 2,898 года. А у 209-го – и вовсе 103 года. Они менее токсичны. А об остальных изотопах и их радиотоксичности практически нет сведений, поскольку они являются короткоживущими.

Как действовать?
То, удастся ли спасти человека от губительного контакта с этим веществом, зависит не от периода полураспада полония-210, и даже не от того, какое количество металла или испарений оказало воздействие. А от лечения и своевременной помощи. Вот как нужно действовать:
- При прикосновении к металлу сразу же промыть этот участок тела, применив большое количество стирального порошка или хозяйственного мыла.
- При попадании изотопа в пищевод надо немедля вызвать рвоту. Поскольку счет идет на секунды, для этого применяются подкожные инъекции апоморфина. И прием слабительного – введение клизмой сульфата натрия и магния.
Естественно, перед этим необходимо вызвать скорую. В таких случаях квалифицированная медицинская помощь первостепенна.
В течении полугода-года изотоп может быть выведен из организма почками. Но за это время он накопится и причинит вред (облысение, например).
Если вещество успело впитаться в ткань органов, медики используют химические соединения из оксатиола и унитиола. Эти препараты могут «извлечь» полоний-210 и вывести наружу. В течение как минимум недели пострадавшему придется лежать под капельницей.
Источники полония
Мало кто знает, но данный изотоп был обнаружен в табаке, используемом при производстве сигарет. И соответственно, в табачном дыме. Производители, конечно же, предпочитают об этом умалчивать. Но данная информация все равно была выяснена и разглашена.
Впервые статью опубликовали в американском издании под названием American Journal of Public Health. Она была написана группой исследователей, в которую вошли специалисты клиники Майо (Рочестер) и ученые Стэнфордского университета.
В статье говорится, что производители сигар более сорока лет тому назад обнаружили, что радиоактивный полоний-210 входит в состав табака. Они всеми доступными методами пытались его изъять из продукции, но безуспешно.
Во избежание большей информированности потенциальных покупателей о данном факте, компании не стали сообщать о результатах своих внутренних исследований. Об этом свидетельствуют внутренние документы концернов табачной промышленности.
Швейцарская газета Le Temps, в свою очередь, пишет о том, что желание скрыть данную информацию было столь сильным, что производители замалчивали ее даже тогда, когда выяснилось – концентрация полония-210 в два-три раза меньше оценок, сделанных изначально.
Ученые считают, что на сигаретных пачках, в связи с этим, необходимо изображать знак, который предупреждал бы о радиоактивной опасности.
Временной интервал в радиоактивности
Момент развала частицы невозможно установить для данного конкретного атома. Для него это скорее «несчастный случай», нежели закономерность. Выделение энергии, характеризующее этот процесс, определяют как активность образца.
 Замечено, что она с течением времени меняется. Хотя отдельные элементы демонстрируют удивительное постоянство степени излучения, существуют вещества, активность которых уменьшается в несколько раз за достаточно короткий промежуток времени. Удивительное разнообразие! Возможно ли найти закономерность в этих процессах?
Замечено, что она с течением времени меняется. Хотя отдельные элементы демонстрируют удивительное постоянство степени излучения, существуют вещества, активность которых уменьшается в несколько раз за достаточно короткий промежуток времени. Удивительное разнообразие! Возможно ли найти закономерность в этих процессах?
Установлено, что существует время, в течение которого ровно половина атомов данного образца претерпевает распад. Этот интервал времени получил название «период полураспада». В чем смысл введения этого понятия?
Получение
В 1 тонне урановой руды содержится изотоп полоний-210 в количестве, равном примерно 100 микрограммам. Их можно выделить при обработке отходов производства, однако для получения более или менее значительного объема элемента пришлось бы обработать огромное количество материала. Гораздо более простым и эффективным способов является синтез с помощью облучения нейтронами природного висмута в ядерных реакторах.
В результате после еще некоторых процедур получается полоний-210. Изотопы 208 и 209 также можно получить, если облучать висмут или свинец ускоренными пучками альфа-частиц, протонов или дейтронов.
Примечания
- Физическая энциклопедия / Гл. ред. А. М. Прохоров. — М.: Советская энциклопедия, 1994. — Т. 4. Пойнтинга — Робертсона — Стримеры. — С. 210. — 704 с. — 40 000 экз. — ISBN 5-85270-087-8.
- Манолов К., Тютюнник В. Биография атома. Атом — от Кембриджа до Хиросимы. — Переработанный пер. с болг.. — М.: Мир, 1984. — С. 20—21. — 246 с.
- А.Н.Климов. Ядерная физика и ядерные реакторы. — Москва: Энергоатомиздат, 1985. — С. 352.
- Бартоломей Г.Г., Байбаков В.Д., Алхутов М.С., Бать Г.А. Основы теории и методы расчета ядерных энергетических реакторов. — Москва: Энергоатомиздат, 1982.
- I.R.Cameron, Nuclear fission reactors. — Canada, New Brunswick: Plenum Press, 1982.
- И.Камерон. Ядерные реакторы. — Москва: Энергоатомиздат, 1987. — С. 320.
Бизнес и финансы
БанкиБогатство и благосостояниеКоррупция(Преступность)МаркетингМенеджментИнвестицииЦенные бумагиУправлениеОткрытые акционерные обществаПроектыДокументыЦенные бумаги — контрольЦенные бумаги — оценкиОблигацииДолгиВалютаНедвижимость(Аренда)ПрофессииРаботаТорговляУслугиФинансыСтрахованиеБюджетФинансовые услугиКредитыКомпанииГосударственные предприятияЭкономикаМакроэкономикаМикроэкономикаНалогиАудитМеталлургияНефтьСельское хозяйствоЭнергетикаАрхитектураИнтерьерПолы и перекрытияПроцесс строительстваСтроительные материалыТеплоизоляцияЭкстерьерОрганизация и управление производством
Примеры характеристик распада
Существующие в природе радиоактивные изотопы в основном возникают в сложных цепочках распадов урана и тория и имеют периоды полураспада в очень широкой области значений: от 3·10−7 секунды для 212Po до 1,4·1010 лет для 232Th. Наибольший экспериментально измеренный период полураспада имеет изотоп теллура 128Te — 2,2·1024 лет. Само существование в настоящее время многих естественных радиоактивных элементов несмотря на то, что с момента образования этих элементов при звёздном нуклеосинтезе прошло более 4,5 млрд лет, является следствием очень больших периодов полураспада 235U, 238U, 232Th и других природных радионуклидов. К примеру, изотоп 238U стоит в начале длинной цепочки (так называемый ), состоящей из 20 изотопов, каждый из которых возникает при α-распаде или β-распаде предыдущего элемента. Период полураспада 238U (4,5·109 лет) много больше, чем период полураспада любого из последующих элементов радиоактивного ряда, поэтому распад в целом всей цепочки происходит за то же время, что и распад 238U, её родоначальника, в таких случаях говорят, что цепочка находится в состоянии секулярного (или векового) равновесия. Примеры характеристик распада некоторых веществ:
| Вещество | 238U | 235U | 234U | 210Bi | 210Tl |
|---|---|---|---|---|---|
| Период полураспада, T12{\displaystyle T_{1/2}} | 4,5·109 лет | 7,13·108 лет | 2,48·105 лет | 4,97 дня | 1,32 минуты |
| Постоянная распада, λ{\displaystyle \lambda } | 4,84·10−18 с−1 | 8,17·10−14 с−1 | 1,61·10−6с−1 | 8,75·10−3 с−1 | |
| Частица | α | α | α | β | β |
| Полная энергия распада, МэВ | 4,2699 | 4,6780 | 4,8575 МэВ | 1,1612 МэВ | 5,482 МэВ |
Примеры
вода
Биологический период полураспада воды у человека составляет от 7 до 14 дней . Это может быть изменено поведением. Употребление большого количества алкоголя снижает биологический период полураспада воды в организме. Это использовалось для обеззараживания людей, внутренне загрязненных тритием водой ( тритием ). Основа этого метода обеззараживания (используемого в Харвелле ) заключается в увеличении скорости, с которой вода в организме заменяется новой.
Алкоголь
Удаление этанола (питьевого алкоголя) путем окисления алкогольдегидрогеназой в печени из человеческого тела ограничено. Следовательно, удаление большой концентрации алкоголя из крови может происходить по . Также этапы ограничения скорости для одного вещества могут быть общими с другими веществами. Например, концентрация алкоголя в крови может использоваться для изменения биохимии метанола и этиленгликоля . Таким образом, можно предотвратить окисление метанола до токсичного формальдегида и муравьиной кислоты в организме человека, если дать соответствующее количество этанола человеку, который проглотил метанол
Обратите внимание, что метанол очень токсичен и вызывает слепоту и смерть. Таким же образом можно лечить человека, который проглотил этиленгликоль
Период полураспада также зависит от субъективной скорости метаболизма рассматриваемого человека.
Общие рецептурные лекарства
| Вещество | Биологический период полураспада |
|---|---|
| Аденозин | Менее 10 секунд |
| Норэпинефрин | 2 минуты |
| Оксалиплатин | 14 минут |
| Сальбутамол | 1,6 часов |
| Залеплон | 1-2 часа |
| Морфий | 2–3 часа |
| Метотрексат | 3–10 часов (меньшие дозы),
8–15 часов (более высокие дозы) |
| Фенитоин | 12–42 часов |
| Метадон | 15–72 часов
В редких случаях до 8 дней |
| Бупренорфин | 16–72 часов |
| Клоназепам | 30–40 часов |
| Флуразепам | 19–100 часов
Активный метаболит ( десфлуразепам ): 1,75–10,4 дня. |
| Диазепам | 20–100 часов
Активный метаболит ( нордазепам ): 1,5–8,3 дня. |
| Донепезил | 3 дня (70 часов) |
| Флуоксетин | 4–6 дней
Активный липофильный метаболит ( сепроксетин ): 4–16 дней. |
| Вандетаниб | 19 дней |
| Амиодарон | 25–110 дней |
| Дутастерид | 35 дней |
| Бедаквилин | 165 дней |
Металлы
Биологический период полураспада цезия у человека составляет от одного до четырех месяцев. Это можно сократить, если накормить человека берлинской лазурью . Берлина в пищеварительной системе действует как твердый ионообменник, который поглощает цезий, высвобождая ионы калия .
Что касается некоторых веществ, важно рассматривать тело человека или животного как состоящее из нескольких частей, каждая из которых имеет собственное сродство к веществу, и каждая часть имеет свой биологический период полураспада ( фармакокинетическое моделирование на физиологической основе ). Попытки удалить какое-либо вещество из всего организма могут привести к увеличению нагрузки, присутствующей в одной части организма
Например, если человеку, загрязненному свинцом, вводят ЭДТА в хелатной терапии , тогда, хотя скорость, с которой свинец теряется из организма, будет увеличиваться, свинец внутри тела имеет тенденцию перемещаться в мозг, где он может это сделать. самый вред.
- Полоний в организме имеет биологический период полураспада от 30 до 50 дней.
- Цезий в организме имеет период биологического полураспада от одного до четырех месяцев.
- Период полураспада ртути (в виде метилртути ) в организме составляет около 65 дней.
- Период полураспада свинца в крови составляет 28–36 дней.
- Свинец в кости имеет период биологического полураспада около десяти лет.
- Кадмий в кости имеет биологический период полураспада около 30 лет.
- Биологический период полураспада плутония в кости составляет около 100 лет.
- Плутоний в печени имеет период биологического полураспада около 40 лет.
Периферический период полураспада
Некоторые вещества могут иметь разный период полураспада в разных частях тела. Например, окситоцин имеет период полураспада в крови обычно около трех минут при внутривенном введении . Периферически вводимые (например, внутривенные) пептиды, такие как окситоцин, очень плохо проникают через гематоэнцефалический барьер , хотя очень небольшие количества (<1%), по-видимому, действительно проникают в центральную нервную систему у людей при введении этим путем. В отличие от периферического введения, при интраназальном введении через назальный спрей окситоцин надежно проникает через гематоэнцефалический барьер и проявляет психоактивные эффекты у людей. Кроме того, в отличие от периферического введения, интраназальный окситоцин имеет центральную продолжительность от 2,25 часа до 4 часов. Вероятно, в связи с этим фактом было обнаружено, что эндогенные концентрации окситоцина в головном мозге в 1000 раз превышают периферические уровни.
Определение и основные соотношения
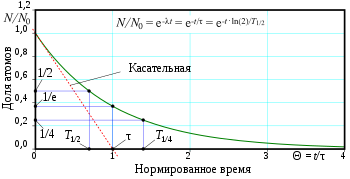
Зависимость числа выживших частиц от времени при экспоненциальном распаде
Понятие периода полураспада применяется как к испытывающим распад элементарным частицам, так и к радиоактивным ядрам. Поскольку событие распада имеет квантовую вероятностную природу, то если рассматривать одну структурную единицу материи (частицу, атом радиоактивного изотопа), можно говорить о периоде полураспада как промежутке времени, по истечении которого средняя вероятность распада рассматриваемой частицы будет равна 1/2.
Если же рассматривать экспоненциально распадающиеся системы частиц, то периодом полураспада T12{\displaystyle T_{1/2}} будет называться время, в течение которого распадается в среднем половина радиоактивных ядер. Согласно закону радиоактивного распада, число нераспавшихся атомов в момент времени t{\displaystyle t} связано с начальным (в момент t={\displaystyle t=0}) числом атомов N{\displaystyle N_{0}} соотношением
- N(t)N=e−λt,{\displaystyle {\frac {N(t)}{N_{0}}}=e^{-\lambda t},}
- где λ{\displaystyle \lambda } — постоянная распада.
По определению, N(T12)N=12,{\displaystyle {\frac {N(T_{1/2})}{N_{0}}}={\frac {1}{2}},} следовательно, e−λT12=12,{\displaystyle e^{-\lambda T_{1/2}}={\frac {1}{2}},} откуда
- T12=ln2λ≈,693λ.{\displaystyle T_{1/2}={\frac {\ln 2}{\lambda }}\approx {\frac {0,693}{\lambda }}.}
Далее, поскольку среднее время жизни τ=1λ{\displaystyle \tau ={\frac {1}{\lambda }}}, то
- T12=τln2≈,693τ,{\displaystyle T_{1/2}=\tau \ln 2\approx 0,693\tau ,}
то есть период полураспада примерно на 30,7 % короче, чем среднее время жизни. Например, для свободного нейтрона T12{\displaystyle T_{1/2}} = 10,3 минуты, а τ{\displaystyle \tau } = 14,9 минуты.
Не следует считать, что за два периода полураспада распадутся все частицы, взятые в начальный момент. Поскольку каждый период полураспада уменьшает число выживших частиц вдвое, за время 2T12{\displaystyle 2T_{1/2}} останется четверть от начального числа частиц, за 3T12{\displaystyle 3T_{1/2}} — одна восьмая и т. д.. При этом для каждой конкретной отдельной частицы по прошествии времени T12{\displaystyle T_{1/2}} ожидаемая средняя продолжительность жизни (соответственно, и вероятность распада, и период полураспада) не изменится — этот контринтуитивный факт является следствием квантовой природы явления распада
Парциальный период полураспада
Если система с периодом полураспада T12{\displaystyle T_{1/2}} может распадаться по нескольким каналам, для каждого из них можно определить парциальный период полураспада. Пусть вероятность распада по i-му каналу (коэффициент ветвления) равна pi{\displaystyle p_{i}}. Тогда парциальный период полураспада по i-му каналу равен
- T12(i)=T12pi.{\displaystyle T_{1/2}^{(i)}={\frac {T_{1/2}}{p_{i}}}.}
Парциальный T12(i){\displaystyle T_{1/2}^{(i)}} имеет смысл периода полураспада, который был бы у данной системы, если «выключить» все каналы распада, кроме i-го. Так как по определению pi≤1{\displaystyle p_{i}\leq 1}, то T12(i)≥T12{\displaystyle T_{1/2}^{(i)}\geq T_{1/2}} для любого канала распада.
Виды частиц, испускаемых при радиоактивном распаде
Э. Резерфорд экспериментально установил (), что соли урана испускают лучи трёх типов, которые по-разному отклоняются в магнитном поле:
- лучи первого типа отклоняются так же, как поток положительно заряженных частиц; их назвали α-лучами;
- лучи второго типа обычно отклоняются в магнитном поле так же, как поток отрицательно заряженных частиц, их назвали β-лучами (существуют, однако, позитронные бета-лучи, отклоняющиеся в противоположную сторону);
- лучи третьего типа, которые не отклоняются магнитным полем, назвали γ-излучением.
Хотя в ходе исследований были обнаружены и другие типы частиц, испускающихся при радиоактивном распаде, перечисленные названия сохранились до сих пор, поскольку соответствующие типы распадов наиболее распространены.
При взаимодействии распадающегося ядра с электронной оболочкой возможно испускание частиц (рентгеновских фотонов, Оже-электронов, конверсионных электронов) из электронной оболочки. Первые два типа излучений возникают при появлении в электронной оболочке вакансии (в частности, при электронном захвате и при изомерном переходе с излучением конверсионного электрона) и последующем каскадном заполнении этой вакансии. Конверсионный электрон испускается в процессе изомерного перехода с внутренней конверсией, когда энергия, выделяющаяся при переходе между уровнями ядра, не уносится гамма-квантом, а передаётся одному из электронов оболочки.
При спонтанном делении ядро распадается на два (реже три) относительно лёгких ядра — так называемые осколки деления — и несколько нейтронов. При кластерном распаде (являющемся промежуточным процессом между делением и альфа-распадом) тяжёлым материнским ядром испускается относительно лёгкое ядро (14C, 16O и т. п.).
При протонном (двухпротонном) и нейтронном распаде ядро испускает соответственно протоны и нейтроны.
Во всех типах бета-распада (кроме предсказанного, но пока не открытого безнейтринного) ядром испускается нейтрино или антинейтрино.
Виды радиоактивного распада: α-распад, β-распад. Характеристики радиоактивных излучений.
Альфа-распад
— самопроизвольное превращение ядра с
испусканием альфа-частицы(ядра гелия)
и квантов λ-излучения.
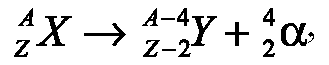
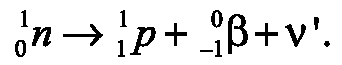
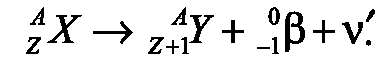
Различают
три вида бета-распада:
-
β-
-распад.
Проявляется в вылете из ядра электрона
(β-)
и антинейтрино. -
β+
-распад.
Образование позитронов и нейтрино.
Энергия,
выделяющаяся при β-распаде, распределяется
между бета-частицей и нейтрино или
антинейтрино.
-
е-захват.
Заключается в захвате ядром одного из
внутренних электронов атома, в результате
чего протон ядра превращается в нейтрон.
Характеристики
радиоактивных излучений.
-
Активность
радиоактивного
препарата – число ядер этого препарата,
распадающихся за секунду.Единица
активности – беккерель (Бк). Наиболее
употребимой единицей является кюри
(Ки). -
Дозой
облучения называется
энергия излучения, поглощенная в единице
объема или массы вещества за все время
воздействия излучения. Доза облучения,
характеризует степень ионизации
вещества: чем больше доза, тем больше
степень этой ионизации. Является мерой
поражающего действия радиоактивных
излучений на организм человека. -
Уровень
радиации (мощность дозы) характеризует
интенсивность излучения. Это доза,
создаваемая за единицу времени и
характеризующая скорость накопления
дозы. Измеряется в рентгенах в час
(Р/ч). Чем больше уровень радиации (фон),
тем меньше времени должны находиться
на загрязненном участке люди, чтобы
полученная ими Доза облучения не
превысила допустимую. -
Степень
загрязнения
радиоактивными веществами характеризуется
плотностью загрязнения, которая
измеряется количеством радиоактивных
распадов атомов, происходящих за единицу
времени на единице поверхности, в
единице массы или объема, т. е. единицами
удельной активности. Знание степени
загрязнения позволяет оценить вредное
биологическое воздействие радиоактивно
загрязненных предметов и веществ при
соприкосновении с ними или попадании
их внутрь организма.