Сероводород, свойства, получение и применение
Содержание:
- Источники
- Мероприятия первой помощи при отравлении
- Отравление сероводородом — симптомы, признаки, первая помощь, класс опасности
- Физические свойства
- Химические свойства
- Что мы узнали?
- Профессиональные вредности
- Применение сероводорода:
- Гибернация у животных и странное вето
- Сероводород — H2S — тотальная коррозия металла
- Примечания[править | править код]
- Получение
- Химические свойства[править | править код]
Источники
Растворимость кислот, оснований и солей в воде
|
Мероприятия первой помощи при отравлении
Химические свойства сероводорода позволяют легко найти противоядие при отравлении — вдыхание кислорода с примесью хлора.
Лечение проводится в отделении интенсивной терапии, где назначается вентиляция легких с созданием положительного давления в дыхательных путях при сильном поражении.
Проводится коррекция ацидоза на основании количества лактата в крови. Симптомы отравления сероводородом схожи с цианидом, потому индуцированная метгемоглобинемия будет препятствовать гипоксии. Пострадавшему вводится 10 мл 3%-ного раствора нитрата натрия за 2-4 минуты, и нужный уровень метгемоглобина достигается за 30 минут. Также внутривенно вводится антисептик метиленовый синий. При бледности кожи и гипотонии лечение дополняется подкожными инъекциями норадреналина, кордиамина и кофеина. Противосудорожная терапия включает закись азота.
При отсутствии реакции на внутривенное введение нитратов или при стойких нарушениях в работе ЦНС используется гипербарическая оксигенация.
При локальном раздражении глаз применение примочек с 3%-ной борной кислотой на глаза, накладывание на веки вазелинового масла, капли новокаина с адреналином в конъюнктивальный мешок.
Профилактика отравлений разрабатывается для опасных производств, где необходимо: контролировать состав воздуха, проводить периодические медосмотры, формировать план действий на случай аварий.
Сероводород крайне редко встречается в природе. Однако в некоторых случаях человек вынужден контактировать с этим веществом. Это происходит не только на работе, но и в быту. Стоит отметить, что незначительная концентрация вещества находится в кишечнике. Невозможно избежать его присутствия в жизни. Что же собой представляет сероводород? Чем опасен для здоровья?
Отравление сероводородом — симптомы, признаки, первая помощь, класс опасности
Запах тухлых яиц с детства напоминает всем о том, что такое сероводород. Бесцветный газ с химической формулой Н2 S легко воспламеняется, во время пожаров он горит синим пламенем.
Ядовитый токсин редко становится причиной острого отравления, но без лечения ухудшает здоровье человека даже в малых дозах. Люди попадают под его воздействие в промышленных условиях, где может гореть кристаллическая сера. Получение вещества в лаборатории осуществляется с помощью газогенератора.
Лечение и профилактика
Лечение проводится в отделении интенсивной терапии, где назначается вентиляция легких с созданием положительного давления в дыхательных путях при сильном поражении.
Проводится коррекция ацидоза на основании количества лактата в крови. Симптомы отравления сероводородом схожи с цианидом, потому индуцированная метгемоглобинемия будет препятствовать гипоксии.
Пострадавшему вводится 10 мл 3%-ного раствора нитрата натрия за 2-4 минуты, и нужный уровень метгемоглобина достигается за 30 минут. Также внутривенно вводится антисептик метиленовый синий.
При бледности кожи и гипотонии лечение дополняется подкожными инъекциями норадреналина, кордиамина и кофеина. Противосудорожная терапия включает закись азота.
При отсутствии реакции на внутривенное введение нитратов или при стойких нарушениях в работе ЦНС используется гипербарическая оксигенация.
При локальном раздражении глаз необходимо применение примочек с 3%-ной борной кислотой на глаза, накладывание на веки вазелинового масла, капли новокаина с адреналином в конъюнктивальный мешок.
Профилактика отравлений разрабатывается для опасных производств, где требуется:
- контролировать состав воздуха;
- проводить периодические медосмотры;
- формировать план действий на случай аварий.
Физические свойства
Каждый человек, анализируя новое для себя вещество, в первую очередь обращает свое внимание на его физические свойства: агрегатное состояние, цвет, запах, прочее. Пожалуй, начать следует именно с запаха сероводорода, он известен всем — тухлые яйца
Конечно, назвать его приятным не сможет никто. Каковы физические свойства сероводорода, не смотря на его распространенность, известно только тем, кто работает с ним или прилежно учился в школе. При стандартных условиях вещество имеет газообразную структуру. Описать физические свойства сероводорода, и при этом не упомянуть об изменении его свойств при температуре свыше 20 градусов по Цельсию было бы огромным упущением, ведь именно при этих условиях возможно полное растворение сероводорода водой. Вода, содержащая это соединение, обладает незначительными кислотными свойствами, диссоциация имеет ступенчатый характер.
Для человека вещество достаточно опасно — оно является своего рода ядом, даже в незначительных количествах. Десятая часть процента газа сероводорода может привести к параличу дыхательных путей человека, что приводит к летальному исходу в течении 8 минут (именно такое время мозг способен жить без поступления нового кислорода).
Ядовитые свойства сероводорода распространяются на всех существ, в крови которых содержится гемоглобин. Железо, в большом количестве содержащиеся в эритроцитах, очень легко вступает в реакцию с молекулами сероводорода, образуя сульфид, который не может переносить кислород.
Противоядие к сероводороду очень просто — нужно всего лишь вдохнуть воздух, насыщенный кислородом и имеющий незначительную примесь хлора, который нейтрализует действие серы. Эксперименты и исследования, связанные с сероводородом должны проводится в специальных условиях.
Химические свойства
Сернистый водород – мощный восстановитель. Основные химические свойства вещества описаны в таблице.
|
Реакция |
Описание |
Уравнение |
|
С кислородом |
Горит на воздухе голубым пламенем с образованием диоксида серы. При недостатке кислорода образуется сера и вода |
– 2H2S + 4O2 → 2H2O + 2SO2; – 2H2S + O2 → 2S + 2H2O |
|
С окислителями |
Окисляется до диоксида серы или серы |
– 3H2S + 4HClO3 → 3H2SO4 + 4HCl; – 2H2S + SO2 → 2H2O + 3S; – 2H2S + H2SO3 → 3S + 3H2O |
|
Со щелочами |
При избытке щёлочи образуются средние соли, при отношении 1:1 – кислые |
– H2S + 2NaOH → Na2S + 2H2O; – H2S + NaOH → NaHS + H2O |
|
Диссоциации |
Ступенчато диссоциирует в растворе |
– H2S ⇆ H+ + HS–; – HS– ⇆ H+ + S2- |
|
Качественная |
Образование чёрного осадка – сульфида свинца |
H2S + Pb(NO3)2 → PbS↓ + 2HNO3 |
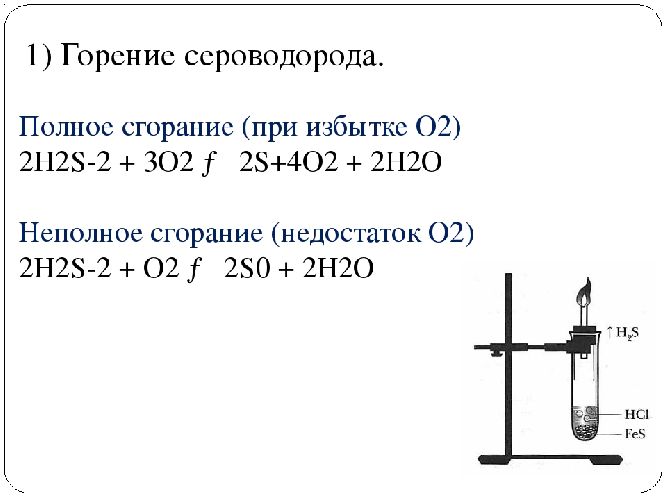
Рис. 3. Горение сероводорода.
Сернистый водород – токсичный газ, поэтому его применение ограниченно. Большая часть производимого сероводорода используется в промышленной химии для производства серы, сульфида, серной кислоты.
Что мы узнали?
Из темы урока узнали о строении, получении и свойствах сероводорода или сернистого водорода. Это бесцветный газ с неприятным запахом. Является токсичным веществом. Образует сероводородную воду, не вступая во взаимодействие с водой. В реакциях проявляет свойства восстановителя. Реагирует с кислородом воздуха, сильными окислителями (оксидами, кислородными кислотами), со щелочами. Диссоциирует в растворе в два этапа. Сернистый водород используется в химической промышленности для изготовления производных веществ.
-
Вопрос 1 из 10
Начать тест(новая вкладка)
Профессиональные вредности
Сероводород сильно ядовит, хотя его токсичность часто недооценивают, напр, при работе в лаборатории. Он является нервным ядом, в высоких концентрациях вызывающим почти мгновенную смерть от паралича дыхательного центра. С. необратимо ингибирует железосодержащие ферменты — цитохромы а, b и с (см. Цитохромы) и цитохромоксидазу (КФ 1.9.3.1), связываясь с железом в их молекулах. Это вызывает острую тканевую гипоксию (см.).
С. поступает в организм преимущественно через дыхательные пути, а также через кожу. В организме он быстро окисляется до элементарной серы и сульфатов, к-рые выводятся с мочой; частично С. выделяется в неизмененном виде через легкие.
Отравления Сероводородом возникают в основном в результате нарушения правил техники безопасности и производственной санитарии (см.), несовершенства технологических процессов, нарушения герметичности оборудования, недостаточной вентиляции производственных помещений, отсутствия или неисправности защитных приспособлений. На степень отравления влияет концентрация С. во вдыхаемом воздухе и длительность воздействия яда. Женщины и подростки более чувствительны к С., чем мужчины. При высоких концентрациях С. опасность отравления им возрастает еще и потому, что при этом запах его человеком не ощущается. Токсический эффект С. усиливается в присутствии углеводородов и сероуглерода.
Порог ощущения запаха С. равен 0,000012—0,00003 мг/л. Незначительный, но явно ощутимый запах отмечают при концентрации С. 0,0014—0,0023 мг/л, сильный запах, но для привыкших к нему не тягостный — при 0,003 мг/л, значительный запах — при 0,004 мг/л, запах тягостный даже для привыкших к нему — при 0,007—0,011 мг/л. При более высоких концентрациях С. запах становится менее сильным и менее неприятным.
Диагностика отравлений С. основывается на данных анамнеза, обстоятельствах отравления и клин, картине.
Хроническое отравление на ранних стадиях характеризуется заболеваниями глаз: болью в глазных яблоках, светобоязнью, слезотечением, конъюнктивитом, появлением мелких точечных дефектов роговицы. На более поздних стадиях хрон. отравления С. наблюдают риниты, ларинготрахеиты, бронхиты, головные боли, общую слабость, снижение слуха, частые головокружения, а также расстройства пищеварения, тошноту, понос, исхудание, анемию, сосудисто-вегетативные нарушения, кожные высыпания, зуд, фурункулез, гнойничковые заболевания кожи, на зубах появляется зеленовато-серый налет. В крови — гипохромная анемия, анизоцитоз, пойкилоцитоз, нейтрофилия.
При хрон. отравлении С. лечение симптоматическое.
Острые отравления Сероводородом делят на легкие, средней тяжести и тяжелые. При легком отравлении на первый план выступают симптомы раздражающего действия С.: жжение в глазах, слезотечение, светобоязнь, бле-фароспазм, покраснение конъюнктивы, насморк, першение в горле, кашель. Возможен рефлекторный спазм бронхов.
При отравлении С. средней тяжести к этим симптомам присоединяются признаки резорбтивного действия яда: головная боль, тошнота, рвота, головокружение, слабость, нарушение координации движений, возбуждение или обморочное состояние. Возможны тахикардия, гипотония, цианоз, поносы, частое мочеиспускание. В моче белок, цилиндры. Температура тела повышена. Иногда могут развиться бронхит или пневмония.
При тяжелом отравлении С. у пострадавшего отмечают синюшность, рвоту, нарушение сердечно-сосудистой деятельности и дыхания, сильное понижение АД. В крови — нейтрофилия, относительное увеличение фракции глобулинов, иногда эритроцитоз. При действии на человека очень высоких концентраций С. (1 мг/л) развивается молниеносная, «апоплектическая», форма отравления — мгновенно наступает потеря сознания, появляются судороги и наступает смерть от паралича дыхательного центра или сердца. Если концентрация С. во вдыхаемом воздухе несколько ниже, отравление проявляется в судорожно-коматозной форме. Иногда кома сменяется двигательным возбуждением, появляются галлюцинации, затем наступает сон. После пробуждения отмечают апатию, сонливость, расстройство памяти. Последствиями перенесенного тяжелого отравления С. могут быть понижение интеллекта вплоть до слабоумия, параличи, хрон. менингит, дистрофия миокарда и др.
Применение сероводорода:
Из-за своей токсичности сероводород находит ограниченное применение:
– в аналитической химии сероводород и сероводородная вода используются как реагенты для осаждения тяжёлых металлов, сульфиды которых очень слабо растворимы;
– в медицине в составе природных и искусственных сероводородных ванн, а также в составе некоторых минеральных вод;
– в химической промышленности для получения серной кислоты, элементной серы, сульфидов;
– в органическом синтезе для получения тиофена и меркаптанов.
В последние годы рассматривается возможность использования сероводорода, накопленного в глубинах Чёрного моря, в качестве энергетического (сероводородная энергетика) и химического сырья.
- https://ru.wikipedia.org/wiki/Сероводород
- https://en.wikipedia.org/wiki/Hydrogen_sulfide
- http://chemister.ru/Database/properties.php?dbid=1&id=818
Примечание: Фото https://www.pexels.com, https://pixabay.com.
Видео https://www.youtube.com/watch?v=RYZkPRGcc0k
карта сайта
Коэффициент востребованности
4 767
Гибернация у животных и странное вето
Ряд исследователей предположили, что, помимо других физиологических ролей, сероводород может использоватья организмом для естественной саморегуляции скорости метаболизма (метаболической активности), температуры тела и потребления кислорода.
Учёных давно интересовала проблема анабиоза (способности приостанавливать жизненные процессы и затем возобновлять их) у человека. Процесс, известный как гибернация или «зимняя спячка», наблюдается в природе у многих видов млекопитающих, а также у жаб. Учёные знали, что, что во время «зимней спячки» у животных продукция эндогенного сероводорода значительно повышается.
Состояние живого организма, при котором жизненные процессы (обмен веществ и др.) настолько замедлены, что отсутствуют все видимые проявления жизни — это вовсе не научная фантастика, а дело времени.
Учёные решили в экспериментах «пойти от противного», и воздействуя небольшими дозами сероводорода на организм млекопитающего, попытаться вызвать замедление метаболических процессов. Как обычно, начали исследования с мышей.
В 2005 году было показано, что мышь можно погрузить в состояние искусственной гипотермии, то есть, почти анабиоза, подвергнув её воздействию низких концентраций сероводорода во вдыхаемом воздухе. В результате дыхание животных замедлялось со 120 до 10 дыхательных движений в минуту, а их температура тела падала с 37 градусов Цельсия до уровня, всего на 2 градуса Цельсия превышающего температуру окружающей среды. Иными словами, эффект был таков, как будто теплокровное животное внезапно становилось холоднокровным.
Учёные посчитали, что теоретически, если бы удалось заставить вызываемую сероводородом гибернацию столь же эффективно работать у людей, это могло бы быть очень полезным в клинической практике для спасения жизни тяжело травмированных или перенёсших тяжёлую гипоксию, инфаркты, инсульты больных, а также для консервации донорских органов.
У мыши, погруженной в подобное состояние примерно на 6 часов, никаких негативных последствий для здоровья, нарушений поведения или каких-либо повреждений внутренних органов обнаружено не было. В 2006 году было также выяснено, что артериальное давление у мыши, подвергнутой подобным образом воздействию сероводорода, также существенно не снижается.
Исследования «сероводородного анабиоза» на теперь уже разных видах животных, продолжались ещё несколько лет, после чего учёные высказали сомнения в том, что эффекта гибернации и гипометаболизма при помощи сероводорода возможно достичь у более крупных животных. В 2008 году тот же эффект на свиньях и овцах воспроизвести не удалось. Это привело исследователей к заключению, что эффект, наблюдаемый у мышей, не наблюдается у более крупных животных, а следовательно, и к человеку применим быть не может.

Однако, в феврале 2010 года руководивший исследованиями учёный Марк Рот заявил на конференции, что вызванная сероводородом гипотермия у человека прошла I фазу клинических испытаний. После чего, в августе 2011 года, ещё до начала набора участников для следующих этапов исследований, решение о проведении дальнейших клинических испытаний на больных с инфарктом было отозвано компанией самого учёного (Ikaria), без объяснения причин.
Сероводород — H2S — тотальная коррозия металла
Сероводород реагирует почти со всеми металлами, образуя сульфиды, которые по отношению к железу играют роль катода и образуют с ним гальваническую пару. Разность потенциалов этой пары достигает 0,2–0,48 В. Способность сульфидов к образованию микрогальванических пар со сталью приводит к быстрому разрушению технологического оборудования и трубопроводов.
Бороться с сероводородной коррозией чрезвычайно трудно: несмотря на добавки ингибиторов кислотной коррозии, трубы из специальных марок нержавеющей стали быстро выходят из строя. И даже полученную из сероводорода серу перевозить в металлических цистернах можно в течение ограниченного срока, поскольку цистерны преждевременно разрушаются из-за растворенного в сере сероводорода. При этом происходит образование полисульфанов HSnH. Полисульфаны более коррозионно-активные элементы, чем сероводород.
Сероводород, присоединяясь к непредельным соединениям, образует меркаптаны, которые являются агрессивной и токсичной частью сернистых соединений — химическими ядами. Именно они значительно ухудшают свойства катализаторов: их термическую стабильность, интенсифицируют процессы смолообразования, выпадения и отложения шлаков, шлама, осадков, что вызывает пассивацию поверхности катализаторов, а также усиливают коррозийную активность материала технологических аппаратов.
H2S значительно усиливает процесс проникновения водорода в сталь. Если при коррозии в кислых средах максимальная доля диффундирующего в сталь водорода составляет 4% от общего количества восстановленного водорода, то в сероводородсодержащих растворах эта величина достигает 40%.
Присутствие в газе кислорода значительно ускоряет процессы коррозии. Опытным путем было найдено, что наиболее коррозионным является такой газ, в котором отношение кислорода к сероводороду составляет 114:1. Это отношение называется критическим.
Наличие влаги в газе влечет коррозию металла, одновременное же присутствие H2S, O2 и H2O является наиболее неблагоприятным с точки зрения коррозии.
Коррозионные действия на металл указанных примесей резко возрастают при увеличении давления.
Скорость коррозии газопроводов прямо пропорциональна давлению газа, проходящего через этот газопровод. При давлении до 20 атм. и влажном газе достаточно даже следов сероводорода 0,002–0,0002% об., чтобы вызвать значительные коррозионные поражения металла труб, ограничивая срок службы газопровода 5–6 годами.
Вследствие коррозионных действий сероводорода, присутствующего в газах, значительно сокращается срок службы силового генерационного оборудования (ГПЭС — ГТУ) и аппаратуры при добыче, транспорте, переработке и использовании газа.
В промысловых условиях особенно большому коррозионному воздействию подвергаются трубы, задвижки, камеры сгорания и поршни силовых установок электростанций, счетчики газа, компрессоры, холодильники.
Значительная часть сероводорода реагирует с металлом и может отложиться в виде продуктов коррозии на клапанах силовых установок, компрессоров, на внутренних стенках аппаратуры, коммуникаций и магистрального газопровода.
Примечания[править | править код]
- ↑
- ↑
- ↑ Ходаков Ю.В., Эпштейн Д.А., Глориозов П.А. § 88. Сероводород // Неорганическая химия: Учебник для 7—8 классов средней школы. — 18-е изд. — М.: Просвещение, 1987. — С. 206—207. — 240 с. — 1 630 000 экз.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4 (Пол-Три). — 639 с. — ISBN 5-82270-092-4.
- ↑
- ↑
- ↑
- . WebMD (2 марта 2009).
- ↑
- ↑
- ↑
- ↑
- ↑
- Mark B. Roth and Todd Nystul. Buying Time in Suspended Animation. Scientific American, 1 June 2005
- .
- . ClinicalTrials.gov (4 ноября 2010). — «This study has been withdrawn prior to enrollment. ( Company decision. Non-safety related )».
- . ClinicalTrials.gov (3 августа 2011). — «This study has been terminated. ( Study Terminated — Company decision )».
- Long-term effects on the olfactory system of exposure to hydrogen sulphide / AR Hirsch and G Zavala Smell and Taste Treatment and Research Foundation, Chicago, IL 60611, USA.
Получение
Сульфид водорода встречается в природе редко. В небольших концентрациях входит в состав попутных, природных, вулканических газов. Моря и океаны содержат сероводород на больших глубинах. Например, сернистый водород находится на глубине 200 метров в Чёрном море. Кроме того, сероводород выделяется при гниении белков, содержащих серу.
В промышленности получают несколькими способами:
- реакцией кислот с сульфидами: FeS + 2HCl → FeCl2 + H2S;
- воздействием воды на сульфид алюминия: Al2S3 + 6H2O → 2Al(OH)3 + 3H2S;
- сплавлением серы с парафином: С18Н38 + 18S → 18H2S + 18С.
Наиболее чистый газ получается при прямом взаимодействии водорода и серы. Реакция протекает при 600°С.
Химические свойства[править | править код]
Собственная ионизация жидкого сероводорода ничтожно мала.
В воде сероводород мало растворим, водный раствор H2S является очень слабой кислотой:
-
- H2S→HS−+H+{\displaystyle {\mathsf {H_{2}S\rightarrow HS^{-}+H^{+}}}}Ka = 6,9⋅10−7 ; pKa = 6,89.
Реагирует со щелочами:
-
- H2S+2NaOH→Na2S+2H2O{\displaystyle {\mathsf {H_{2}S+2NaOH\rightarrow Na_{2}S+2H_{2}O}}} (средняя соль, при избытке NaOH)
- H2S+NaOH→NaHS+H2O{\displaystyle {\mathsf {H_{2}S+NaOH\rightarrow NaHS+H_{2}O}}} (кислая соль, при отношении 1:1)
Сероводород — сильный восстановитель. Окислительно-восстановительные потенциалы:
-
- S+2e−→S2−(Eh=−0.444B){\displaystyle {\mathsf {S+2e^{-}\rightarrow S^{2-}(Eh=-0.444B)}}}
- S+2H++2e−→H2S(Eh=0.144B){\displaystyle {\mathsf {S+2H^{+}+2e^{-}\rightarrow H_{2}S(Eh=0.144B)}}}
В воздухе горит синим пламенем:
-
- 2H2S+3O2→2H2O+2SO2↑{\displaystyle {\mathsf {2H_{2}S+3O_{2}\rightarrow 2H_{2}O+2SO_{2}\uparrow }}}
при недостатке кислорода:
-
- 2H2S+O2→2S+2H2O{\displaystyle {\mathsf {2H_{2}S+O_{2}\rightarrow 2S+2H_{2}O}}} (на этой реакции основан промышленный способ получения серы).
Сероводород реагирует также со многими другими окислителями, при его окислении в растворах образуется свободная сера или ион SO42−, например:
-
- 3H2S+4HClO3→3H2SO4+4HCl↑{\displaystyle {\mathsf {3H_{2}S+4HClO_{3}\rightarrow 3H_{2}SO_{4}+4HCl\uparrow }}}
- 2H2S+SO2→2H2O+3S{\displaystyle {\mathsf {2H_{2}S+SO_{2}\rightarrow 2H_{2}O+3S}}}
- H2S+H2O2→2H2O+S{\displaystyle {\mathsf {H_{2}S+H_{2}O_{2}\rightarrow 2H_{2}O+S}}}
Качественной реакцией на сероводородную кислоту и её соли является их взаимодействие с солями свинца, при котором образуется чёрный осадок сульфида свинца, например:
-
- H2S+Pb(NO3)2→PbS↓+2HNO3{\displaystyle {\mathsf {H_{2}S+Pb(NO_{3})_{2}\rightarrow PbS{\downarrow }+2HNO_{3}}}}
При пропускании сероводорода через человеческую кровь она чернеет, поскольку гемоглобин разрушается и железо, входящее в его состав и придающее крови красный цвет, вступает в реакцию с сероводородом и образует чёрный сульфид железа.
Сульфидыправить | править код
Соли сероводородной кислоты называют сульфидами. В воде хорошо растворимы только сульфиды щелочных металлов, аммония. Сульфиды остальных металлов практически не растворимы в воде, они выпадают в осадок при введении в растворы солей металлов и растворимой соли сероводородной кислоты, например сульфида аммония (NH4)2S. Многие сульфиды ярко окрашены.
Для всех щелочных и щелочноземельных металлов известны также гидросульфиды M+HS и M2+(HS)². Гидросульфиды Са2+ и Sr2+ очень нестойки. Являясь солями слабой кислоты, в водном растворе растворимые сульфиды подвергаются гидролизу. Гидролиз сульфидов, содержащих металлы в высоких степенях окисления, либо гидроксиды которых являются очень слабыми основаниями (например, Al2S3, Cr2S3 и др.), часто проходит необратимо с выпадением в осадок нерастворимого гидроксида.
Сульфиды применяются в технике, например полупроводники и люминофоры (сульфид кадмия, сульфид цинка), смазочные материалы (дисульфид молибдена) и др.
Многие природные сульфиды в виде минералов являются ценными рудами (пирит, халькопирит, киноварь, молибденит).
Пример окисления сульфида перекисью водорода:
-
- PbS+4H2O2=PbSO4+4H2O{\displaystyle {\mathsf {PbS+4H_{2}O_{2}=PbSO_{4}+4H_{2}O}}}